
(세종=세종충청뉴스) 송윤영 기자 = KAIS는 바이오및뇌공학과 정기훈 교수 연구팀이 *나노 플라즈모닉 구조를 통해 빠른 열 순환 및 실시간 정량 분석이 가능한 초고속 실시간 중합효소연쇄반응(PCR) 기술을 개발했다고 7일 밝혔다.
▶ 나노 플라즈모닉 구조(Nanostructures for Plasmonic): 빛의 파장보다 작은 크기의 금속나노구조이며, 빛이 표면에 조사될 때 금속 표면과 유전체의 경계에서 빛과 전자가 상호작용을 한다. 주로 바이오 물질의 검출이나 분자진단에 많이 응용된다.
최근 코로나19를 포함한 전염성이 높은 바이러스의 확산을 방지하기 위해 신속하고 정확하게 바이러스를 검출하는 기술이 절실하게 필요하다. 역전사 중합효소연쇄반응(RT-PCR)은 가장 표준화된 코로나19 진단법으로 바이러스 내부의 유전물질인 RNA를 상보적 DNA로 역전사한 후 타겟 DNA를 증폭해 형광 프로브로 검출하는 방법이다. 그러나 기존 RT-PCR은 높은 민감도와 정확도를 갖추지만, 검출 시간이 길고 고가의 대형장비를 갖춘 장소로 검체를 운송한 후 진단하는 등 실시간 현장 대응의 한계가 존재한다.
연구팀이 개발한 `실시간 나노 플라즈모닉 PCR'은 백색 발광다이오드(LED)의 높은 광 흡수율을 갖는 나노 플라즈모닉 기판에 진공 설계된 미세 유체칩을 결합해 소량의 검체를 신속하게 증폭하고 정량적으로 분석해 바이러스를 단시간 내에 정확하게 검출할 수 있다. 이러한 특징을 이용해 공공장소 등 환자 발생 장소에서 병원성 바이러스의 확산 및 해외유입을 차단할 수 있을 것으로 기대된다.
나노 플라즈모닉 기판은 유리 나노기둥 위 금 나노섬 구조로 가시광선 전 영역에서 높은 광 흡수율을 가지므로 백색 LED의 빛을 열에너지로 치환해 빠르게 열을 발생시키고 내보낼 수 있다. 또한 광열 발생장치의 수직적인 온도 구배로 인한 증폭 효율 저하를 해결하기 위해 연구팀은 진공 설계된 미세 유체칩을 결합했다.
이는 샘플 한 방울을 칩에 넣으면 진공이 액체를 마이크로 챔버로 잡아당겨 자동으로 3분 이내에 주입되고, PCR 과정 동안에 발생하는 미세 기포는 공기 투과성 벽을 통해 제거돼 PCR 효율을 높이는 원리다.
연구팀은 SARS-CoV-2 플라스미드 DNA를 사용해 해당 기술을 검증했고, 40싸이클(95도-60도)을 5분 이내에 수행해 타겟 바이러스를 91%의 증폭 효율과 함께 정량적으로 검출했다. 이는 기존 실시간 PCR 시스템의 긴 소요 시간(약 1시간)에 비해 매우 빠르고, 높은 증폭 효율을 보이므로 신속한 현장 진단에 적용되기 적합할 것으로 보인다.
정기훈 교수는 "실질적으로 현장에서 사용 가능한 초고속 분자진단법을 개발했다ˮ며 "이 실시간 나노 플라즈모닉 PCR 기술은 현장에서 분자진단을 위한 차세대 유전자 증폭 플랫폼을 제공할 것이며 바이러스 확산 방지에 기여할 수 있을 것으로 예상한다ˮ라고 말했다.
KAIST 바이오및뇌공학과 강병훈 박사과정이 주도한 이번 연구 결과는 국제 학술지 `에이씨에스 나노 (ACS Nano)'에 지난 5월 19일 字로 게재됐다. (논문명: Ultrafast and Real-time Nanoplasmonic On-Chip Polymerase Chain Reaction for Rapid and Quantitative Molecular Diagnostics)
한편 이번 연구는 KAIST 코로나19대응 과학기술뉴딜사업단과 한국연구재단 개인연구지원사업, 바이오기술개발사업으로 수행됐다.


□ 연구개요
연구배경
현재 신·변종 바이러스는 대부분 조기진단 및 백신 치료제 등의 개발이 미흡해 실효성 있는 대응책이 존재하지 않는다. 따라서 해외유입 감염병 확산으로부터 인류의 공중보건을 지키기 위해서는 바이러스의 감염여부를 신속하게 판단하고, 환자의 적절한 치료를 위해 병원체 감별을 위한 공항, 선별진료소 등 현장진단용 초소형 PCR기반 분자진단기기 및 랩온어칩이 필요하다. 기존 검사장비가 대체로 고가의 대형장비로서 이동할 수 없어 검체의 수집과 운송문제로 검사에 제약이 있다. 또한, 시료준비 및 장비 조작, 결과분석이 복잡하여 전문기술을 보유한 전담인력이 필요하고 검사시간이 4시간 이상 소요되는 문제점이 있어 현장진단이 가능한 분자진단이 절실히 필요하다.
연구내용
유리나노기둥위 금나노섬 구조는 댜양한 크기의 나노섬과 다양한 나노갭들로 구성되어 있어 가시광선 전 영역에서 높은 광 흡수율을 나타내므로 백색 LED의 빛을 높은 효율로 열로 치환할 수 있다. 이를 통해 백색 LED를 키면 기판의 온도가 매우 빠르게 올라가고 백색 LED를 끄면 기판의 온도가 빠르게 냉각되며, PCR의 빠른 온도싸이클을 획득할 수 있다. 기판으로부터 수직적으로 균일한 온도를 형성하기 위해 미세유체 칩을 결합하였으며 진공 설계를 통해 샘플의 빠른 자동주입이 가능하고 PCR 동안에 발생하는 미세 기포를 효율적으로 제거할 수 있어 높은 증폭효율을 나타낸다. 이 연구에서는 나노플라즈모닉 구조와 미세유체 채널을 결합하여 초고속 실시간 나노플라즈모닉 PCR 기술을 개발하였다 (그림 1).
양산이 가능한 Microelectromechanical systems (MEMS) 공정 방법인 금속증착 및 식각을 통해 나노플라즈모닉 구조를 대면적으로 제작하였으며, 이후 미세유체채널을 결합하여 실시간 나노플라즈모닉 PCR용 칩을 완성하였다 (그림 2). 완성된 칩은 14 x 26 x 4 mm로 매우 작은 사이즈이며, 백색 LED로부터 최대 200도까지 빠르게 열을 발생시킬 수 있다.
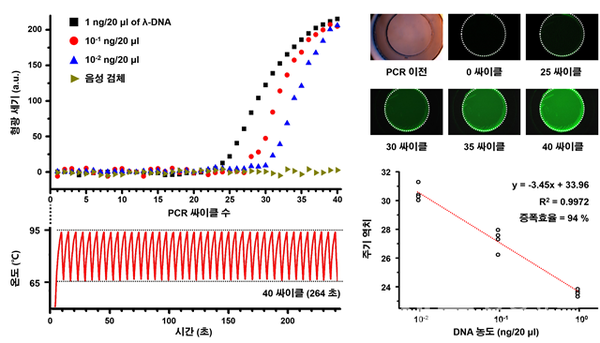
완성된 나노플라즈모닉 PCR용 칩을 활용하여 람다 DNA를 타겟으로 검증하였고 40싸이클(95~65도) 기준 264초 이내에 증폭하고 실시간으로 형광신호를 통해 정량화하였다 (그림 3). 싸이클마다 촬영된 형광 이미지의 형광 세기는 싸이클이 올라감에 따라 PCR 표준곡선과 유사하게 증가함을 확인하였고 94 %의 증폭효율을 나타냈다.
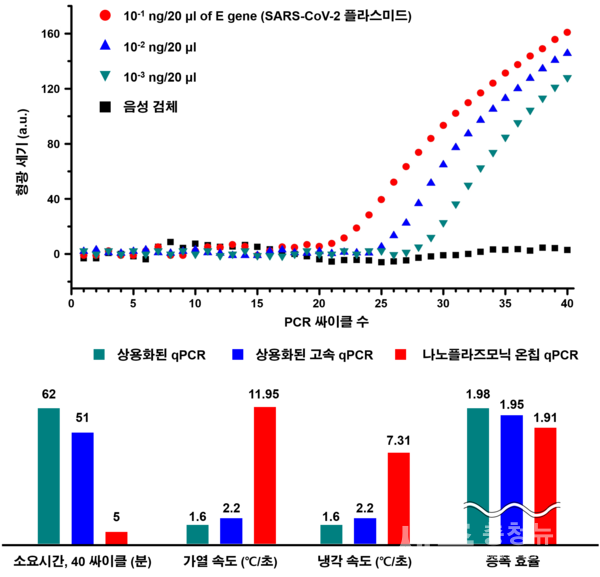
코로나 19 테스트를 위해 SARS-CoV-2 플라스미드 DNA를 활용하여 실시간 플라즈모닉 PCR 기술을 검증하였고, 40싸이클(95도~60도) 기준 5분 이내에 증폭 및 정량화에 성공하였다 (그림 4). 기존 실시간 PCR 시스템과 비교 결과 실시간 나노플라즈모닉 PCR은 검출 소요 시간을 매우 단축시켰으며 유사한 증폭효율을 나타냄을 확인하였다.


