다양한 고형암에서 적용 가능한 플랫폼으로 기존의 항암 면역치료의 효과를 증진 시킬 것으로 기대

(대전=세종충청뉴스) 송윤영 기자 = 암은 현대인의 건강을 위협하는 대표적인 질병으로 꼽히고 있다. 최근의 암 연구 중에서 가장 많은 진전이 있었던 분야는 암 환자가 갖고 있는 면역체계를 활용해 암을 극복하는 면역 항암치료다. 여기 기존의 모든 항암 치료에 불응한 말기 고형암 환자들에게 적용 가능한 차세대 면역 항암 치료법이 개발되어 화제다.
카이스트(총장 이광형)는 생명과학과 김찬혁 교수 연구팀이 면역시스템이 억제되는 종양미세환경을 극복하는 ‘2세대 T세포 수용체 T (T cell receptor specific T, 이하 TCR-T) 세포’ 치료제를 개발했다고 20일 밝혔다.
연구팀은 유전자 조작을 통해 암세포를 직접 파괴할 수 있도록 하는 TCR-T 세포 치료제 제작에 크리스퍼-캐스9 유전자 편집 기술을 이용해 T 세포 수용체 신호전달의 핵심적인 CD247 유전자에 추가신호 전달체인 트레프2-결합 도메인이 포함되도록 개량했다. 이러한 유전자 편집을 통한 개량은 TCR-T 세포의 증식 및 지속성을 향상시켰고, 생쥐를 이용한 악성 흑색종 모델에서 탁월한 항암 효과를 보임을 확인했다.
카이스트 생명과학과 나상준 박사와 김세기 박사가 공동 제1 저자로 참여한 이번 연구는 국제 학술지 '저널 포 이뮤노쎄라피 오브 캔서 (Journal for Immunotherapy of Cancer)'에 지난 4월 5일 출판됐다. (논문명: Engineering second-generation TCR-T cells by site-specific integration of TRAF-binding motifs into the CD247 locus)
초기 미비한 항암 효과를 보이던 1세대 키메라 항원 수용체 (chimeric antigen receptor, 이하 CAR)를 장착한 CAR-T 세포와 다르게, 추가신호 전달체가 포함된 2세대 CAR-T 세포는 말기 백혈병 환자들을 대상으로 80% 이상의 높은 치료 효과를 보이며 ‘기적의 항암제’로 불리고 있다. 하지만 현 CAR-T 치료제는 B세포성 급성 백혈병과 다발 골수종 같은 혈액암에만 치료 효과가 국한돼 있으며, 고형암 환자들을 대상으로 높은 치료효과를 보이는 CAR-T 치료제가 아직까지 없다는 점이 해결해야 할 과제로 대두되고 있다. 또한 TCR-T 치료제는 CAR-T와는 다르게 아직 1세대 구조에 머물고 있다.
이러한 관점에서, 연구진은 고형암을 표적으로 하는 TCR-T 세포에 추가 신호 전달체인 트레프2-결합 도메인이 포함된 2세대 TCR-T 세포 치료제를 개발했다. 단일 단백질로 이뤄진 CAR와 다르게 단백질 복합체를 형성하는 TCR에 추가신호 전달체를 포함시키는 엔지니어링은 훨씬 도전적이다. 연구진은 다양한 시도 끝에 TCR의 형성과 기존 신호전달에 영향을 주지 않으면서 동시에 추가 신호가 유발되는 최적의 TCR 모듈을 구축했다.
제1 저자인 나상준 박사는 “고형암이 형성하는 면역억제 환경에서, 기존 1세대 TCR-T 세포의 항암효과는 제한될 수 밖에 없다”라며 “반면 2세대 TCR-T 세포는 면역억제 환경에서도 지속적인 항암효과를 유지하도록 고안된 기술 전략으로, 기존 치료제의 효과를 기대하기 어려운 고형암 환자들에게 필요한 치료제가 될 것으로 기대한다”라고 말했다.
이번 연구는 삼성전자 미래기술육성센터의 지원을 받아 수행됐다.
붙임 : 연구개요, 그림 설명,
암의 치료 방법 중에서 면역 항암 요법은 뛰어난 치료 효과와 낮은 부작용으로 인해 차세대 치료제로서 각광을 받고 있다. 이 중 면역세포 치료제인CAR-T 세포는 B세포성 급성 백혈병과 다발 골수종 환자들을 대상으로 높은 항암 효과를 보이며, 2017년 미국에서 최초로 2종의 CAR-T 세포 (Kymriah, Yescarta)가 치료제 허가를 승인 받았다. 이후 2023년 현재까지 6종의 CAR-T 치료제가 미국 식약처의 승인을 받았다. 이들은 모두 2세대 CAR-T 세포로서 T세포 수용체 신호 전달 도메인만을 포함하는 1세대 CAR-T와 다르게 추가적으로 보조자극 수용체의 신호 전달 도메인을 포함으로써 더욱 향상된 항암 효과를 갖는다. 또다른 면역세포 치료제인 TCR-T 세포는 세포 내 항원도 인식이 가능하므로 고형암의 표적에 용이성을 갖고 있다. 하지만 고형암이 형성하는 면역억제 환경으로 인하여 TCR-T 세포의 항암효과는 크게 저해를 받는다. 본 연구진은 CAR-T의 개발 과정에서 얻은 교훈을 차세대 TCR-T 세포 치료제 개발 과정에도 적용하여 추가신호 전달체가 포함한 2세대 TCR-T 플랫폼을 개발하였다.
2. 연구내용
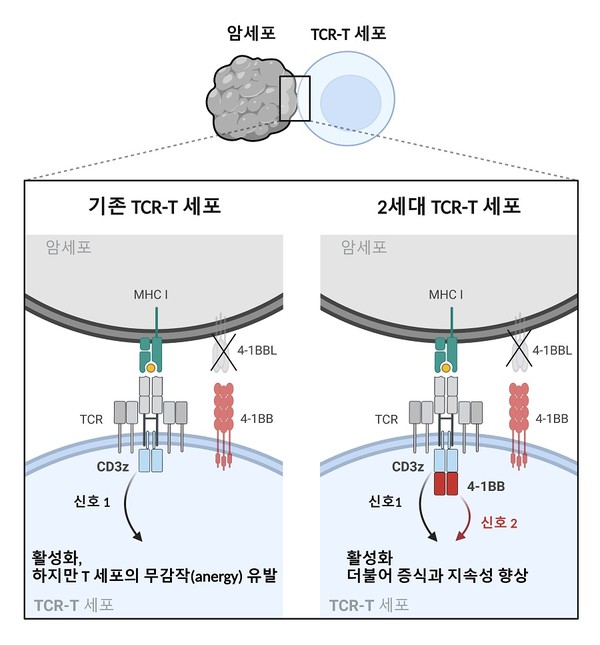
TCR-T 세포는 고형암을 치료하기 위해 대두되는 항암 면역치료제이다. 그러나 추가신호전달을 받을 수 없는 고형암의 면역억제 환경에서 TCR-T 세포의 증식과 효능이 제한될 수 밖에 없다. 이러한 문제를 극복하고자 TCR 복합체 내에서 신호 전달에 핵심적인 역할을 하는 단백질인 CD3z의 유전자 (=CD247)에 보조자극 수용체인 4-1BB의 신호도메인인 TRAF2-결합 모티프 (TRAF2-binding motifs, 이하 TBM)가 삽입된 퓨전 CD3z 모듈을 구축하였다. 이 과정에서 CD247 유전자 내에 4-1BB 신호도메인이 삽입 위치에 따라 신호전달 강도에 변화가 있음을 밝혔다. 더 나아가 4-1BB 신호도메인의 삽입에 따른 CD3z 수용체의 전하적 특성의 변화가 TCR복합체의 형성과 신호 전달을 중요한 영향을 미치는 것을 새롭게 발견하였다. 이를 통해 기존 TCR 신호전달의 손상 없이 4-1BB 추가신호전달이 동시에 유발되는 최적의 CD3z 모듈을 구축하였다. 최적화된 CD3z 모듈이 적용된 2세대 TCR-T 세포는 증식 및 지속성을 향상시켰을 뿐만 아니라, 생쥐를 이용한 악성 흑생종 모델에서 기존의 1세대 TCR-T 세포보다 더 증진된 항암 효과를 보였다.
3. 기대효과
2세대 TCR-T 세포 치료제는 악성 흑색종 뿐만 아니라 다양한 고형암을 대상으로 확장될 수 있다. 또한 2세대 TCR-T 세포에 적용된 CD3z 모듈은 TCR-T 치료제 뿐만 아니라 종양 침윤 림프구 (Tumor Infiltrating Lymphocytes, TIL)와 바이러스-특이적 T 세포 (virus-specific T cells, VST) 치료제에도 적용이 가능한 플랫폼이다. 이러한 형태의 치료제 플랫폼은 현재 고형암이 갖고 있는 가장 큰 문제인 면역억제환경과 항원 이질성을 모두 극복할 수 있는 가능성이 있음을 시사한다.